
Авторы: Эседова Асият Эседовна – профессор, д.м.н.;
Идрисова Муминат Абдусаламовна – аспирант.
ФГБОУ ВО «Дагестанский государственный медицинский университет» МЗ РФ,
Республика Дагестан, г. Махачкала, ул. Ленина,1.
Содержание
Коррекция костно-метаболических нарушений у женщин в постменопаузе на фоне тиреоидной патологии препаратом «Остеомед Форте»
Введение
Главная проблема современного общества, которую выделяют многие социологи, – это способность человека вести «независимую жизнь». Это особенно актуально для лиц пожилого возраста, у которых «независимая жизнь» тесно связана с психической сохранностью и способностью к движению, что дает возможность самообслуживанию. Население планеты стареет, продолжительность жизни увеличивается, и современная женщина более трети жизни проводит в постменопаузе. Как известно, распространенность постменопаузального остеопороза (ПМОП) в России составляет 30,5-33,1%, причем, женщины с возрастом могут терять до 50% губчатой и 35% компактной кости. ПМОП представляет собой одну из основных проблем здравоохранения в развитых странах. Приблизительно у каждой третьей женщины после 65 лет наблюдается как минимум один остеопоротический перелом костей [1].
Отдельную группу риска развития остеопороза (ОП) в постменопаузе образуют больные, страдающие заболеваниями тиреоидной системы. Как известно, гипотиреоз является наиболее типичным проявлением йоддефицитных заболеваний в эндемичных зонах, которых в России более 50% территории (Урал, некоторые регионы Сибири, Центрально – Европейская часть, Север, Среднее и верхнее Поволжье, Северный Кавказ и др.) [2].
При дефиците тиреоидных гормонов, являющихся необходимыми для формирования и функционирования организма человека, развиваются тяжелые изменения всех органов и систем, в том числе и со стороны костной системы. У пациентов с гипотериозом замедлено костное ремоделирование – в 2-3 раза снижена скорость обеих составляющих ремоделирующего цикла – костной резорбции и костного формирования [3].
Поскольку при ПМОП в основе наблюдаемых изменений в костях лежит ослабление костно-протективного эффекта половых стероидов на фоне их недостаточности, менопаузальную гормональную терапию (МГТ) препаратами женских половых стероидов вполне обосновано можно рассматривать, как «первую линию» лечебных воздействий, направленных на обеспечение сохранности костной ткани, в условиях возникшей гипоэстрогенемии. Однако, учитывая ряд серьезных побочных эффектов МГТ, таких как венозная тромбоэмболия, рак молочной железы, артериальный тромбоз и др. и наличие широкого спектра противопоказаний, возникает необходимость в поиске альтернативного препарата для купирования костно-метаболических нарушений на фоне тиреоидной патологии у женщин в постменопаузе.
Учитывая принципиальную разницу между двумя препаратами: Анжелик и Остеомед Форте, представляется интересным сравнить их эффективность во влиянии на костную ткань.
Цель исследования
Оценить эффективность препарата Остеомед Форте в лечении ПМОП у женщин с тиреоидной патологией.
Материалы и методы исследования
В исследование включено 265 женщин в состоянии физиологической постменопаузы. Средний возраст обследованного контингента женщин составил 57,0±0,73 года, длительность постменопаузы не превышала 14 лет (средняя длительность постменопаузы 8,4±1,53 года). Женщины были разделены на две группы: в 1 группу (основную) вошли 165 женщин с медикаментозно компенсированным гипотиреозом на фоне аутоиммунного тиреоидита (АИТ) и эндемического зоба (ЭЗ), во 2 группу (контрольную) – 100 женщин без тиреоидной патологии. В 1 группе обследуемых назначение препаратов МГТ проводилось на фоне ранее компенсированного L-тироксином гипотиреоза. В дальнейшем в исследовании участвовало 165 женщин с медикаментозно компенсированным гипотиреозом на фоне АИТ и ЭЗ. Данная группа женщин была разделена, в свою очередь, на две подгруппы:
- 82 женщины получали терапию препаратом Анжелик;
- 83 женщины – терапию препаратом Остеомед Форте.
Минеральную плотность кости (МПК) определяли методом двухэнергетической рентгеновской абсорциометрии (ДЭРА) с помощью аппарата Lunar Prodigy в поясничном отделе позвоночника (L1 – L4), шейке бедренной кости (Neck), большом вертеле (Troch), треугольнике Варда (Ward). Диагностика остеопороза осуществлялась согласно критериям ВОЗ (1994) по Т-критерию, т.е. в стандартных отклонениях (SD) от нормативных показателей пиковой костной массы здоровых женщин. Величина SD до 1 расценивалась как норма, от 1 до 2,5 SD – как остеопения, ниже 2,5 SD – как остеопороз.
Состояние кальций – фосфорного обмена определяли с помощью ионселективного электрода на анализаторе электролитов Микролит 3+2 фирмы «Kone» (Финляндия). Уровень экскреции кальция (метод Arsenazo III), фосфора (метод Molyb date), креатинина (метод Jaffe) определяли с помощью коммерческих наборов фирмы «Kone» (Финляндия) на биохимическом анализаторе Konelab – 30.
Костный обмен характеризовали по уровню биохимических маркеров костного ремоделирования. О состоянии костного формирования судили по содержанию в сыворотке крови остеокальцина (ОК), которое определяли иммунорадиометрическим методом с помощью набора Cis Bio International (Франция), и содержанию костной щелочной фосфатазы (КЩФ), которое определяли иммуноферментным методом с использованием моноканальных антител с помощью коммерческих наборов Аlkphase-B (США). Состояние костной резорбции оценивали посредством определения уровня С-концевых телопептидов (СТх), образующихся при деградации коллагена I типа во второй утренней порции мочи и в сыворотке крови иммуноферментным методом с использованием тест-систем Cross Laps ELISA фирмы «Osteometer Bio Tech». Активность костной резорбции также определяли колориметрическим методом по экскреции оксипролина (ОПР) – ОПР с мочой натощак по отношению к экскреции креатинина (Кр) (ОПР/Кр, мкг/мкмоль/Кр).
Результаты исследования обрабатывали при помощи пакета статистических программ Microsoft Excel-98, при этом соблюдались общие рекомендации для медицинских и биологических исследований [4]. Определялись средние арифметические величины (М) и их ошибки (m). С целью выявления значимости (достоверности) различий сопоставляемых средних величин применялся t-критерий Стьюдента и F-критерий Фишера с учетом неоднородности дисперсий в исследуемых группах. Разница средних величин считалась достоверной при р<0,05. Для определения характера связи между изучаемыми параметрами применялся корреляционный анализ с вычислением коэффициента корреляции r и последующим установлением его значимости по критерию t Стьюдента [5], а также использовались коэффициенты линейной корреляции Пирсона, коэффициент ранговой корреляции Спирмена. Для оценки вклада ряда клинико-инструментальных и лабораторных показателей в снижение костной массы было использовано регрессионное моделирование с расчетом многомерных пошаговых регрессий.
Все участники проведенного исследования подписали информированное согласие. Протокол исследования №6 одобрен этическим комитетом «Дагестанского государственного медицинского университета» от 23.09.2015 г.
Таблица 1
Общая схема исследования
| Фон | Исходно | 3 мес. | 6 мес. | 12 мес. |
| Общеклиническое обследование | + | + | + | + |
| ТТГ | + | + | + | + |
| Т3 | + | + | + | + |
| Т4 СВ | + | + | + | + |
| Пролактин | + | – | + | + |
| ФСГ | + | – | + | + |
| ЛГ | + | – | + | + |
| Эстрадиол | + | – | + | + |
| Прогестерон | + | – | + | + |
| Кальцитонин | + | – | + | + |
| Паратиреоидный гормон | + | – | + | + |
| УЗИ щитовидной железы | + | – | + | + |
| УЗИ гениталий | + | – | – | + |
| Маммография | + | – | – | + |
| ДЭРА | + | – | – | + |
| Маркеры резорбции кости в моче – ОПР, СТХ; в крови – СТХ | + | + | + | + |
| Маркеры образования кости в сыворотке крови – КЩФ, ОК, ЩФ | + | + | + | + |
| Са, Р в крови | + | + | + | + |
| Креатинин в моче | + | + | + | + |
| Са, Р в моче | + | + | + | + |
| Гемостазиограмма | + | – | + | + |
| Йод в моче | + | – | + | + |
Примечание: «+» – показатель определен, «-» – показатель не определялся
Таблица 2
Динамика показателей МПК в различных сегментах скелета в течение года на фоне приема препаратов Анжелик (1-ая подгруппа) и Остеомед Форте (2-ая подгруппа) (М±m)
| Сегмент скелета | Единицы измерения | 1 подгруппа (N=82) | 2 подгруппа (N=83) | ||
| Исходный уровень | После 12 месяцев | Исходный уровень | После 12 месяцев | ||
| L1-L4 | г/см2 | 0,882±0,12 | 0,941±0,18 | 0,887±0,11 | 0,917±0,16* |
| Z (%) | 75,1±14,3 | 85,1±15,7 | 75,6±14,1 | 79,43±14,6* | |
| T (SD) | -2,52±1,5 | -1,37±0,96* | -2,52±1,3 | -1,94±0,93* | |
| Neck | г/см2 | 0,706±0,10 | 0,731±0,11 | 0,714±0,13 | 0,738±0,11 |
| Z (%) | 83,7±10,7 | 86,36±11,2 | 84,1±10,6 | 87,96±12,1* | |
| T (SD) | -1,71±0,93 | -1,54±0,91 | -1,65±0,99 | -1,34±1,2 | |
| Troch | г/см2 | 0,612±0,14 | 0,629±0,11 | 0,618±0,12 | 0,645±0,15 |
| Z (%) | 80,6±12,1 | 84,5±12,9 | 80,8±14,7 | 85,6±13,8* | |
| T (SD) | -2,20±0,92 | -2,01±0,99 | -2,14±1,2 | -1,79±0,98 | |
| Ward | г/см2 | 0,555±0,13 | 0,579±0,11 | 0,563±0,14 | 0,583±0,13 |
| Z (%) | 76,4±14,8 | 80,3±12,3 | 76,6±15,9 | 78,5±14,6* | |
| T (SD) | -2,76±1,3 | -2,15±1,1 | -2,70±1,2 | -2,28±1,5 | |
| Total body | г/см2 | 0,876±0,18 | 0,908±0,16 | 0,882±0,14 | 0,915±0,12 |
| Z (%) | 86,1±11,9 | 90,4±14,7 | 86,3±11,4 | 89,6±14,3* | |
| T (SD) | -1,41±0,99 | -0,96±0,92 | -1,35±0,98 | -0,93±0,91 | |
| Дистальный отдел предплечья | г/см2 | 0,807±0,11 | 0,837±0,13 | 0,813±0,14 | 0,849±0,12 |
| Z (%) | 85,0±9,7 | 87,81±9,5 | 85,2±10,1 | 89,01±11,2* | |
| T (SD) | -1,63±0,97 | -1,26±1,03 | -1,57±1,2 | -1,07±0,99 | |
Примечание: * – различия с контрольной группой достоверны (р<0,05)
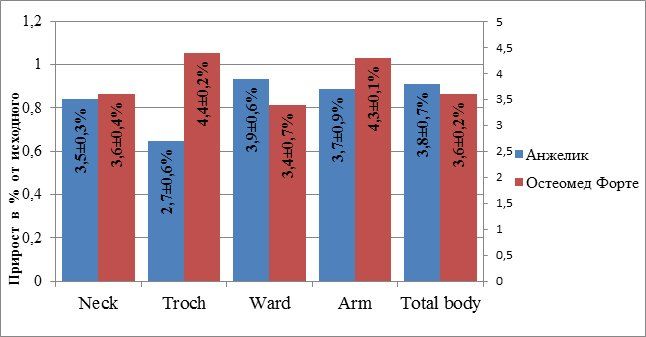
Рисунок 1. Динамика МПК в различных сегментах скелета на фоне двух видов терапии (М±m)
Интересен тот факт, что если протективный эффект Анжелика более выражен в отношении трабекулярных костных структур (L1-L4), то защитный эффект Остеомеда Форте превалирует в отношении кортикальных (проксимальный отдел бедра, дистальный отдел предплечья) (рисунок 1). Это приобретает особую актуальность, учитывая увеличение частоты переломов шейки бедра у пациенток в постменопаузе и сенильном периоде, огромные затраты на восстановление и высокий процент летальности. Как известно, наибольший риск смерти после перелома бедра возникает в первые 3–6 месяцев и составляет от 12 до 24%. Летальность в течение первого года после перелома в различных регионах страны колеблется от 30,8 до 35,1%, причем из выживших больных спустя год нуждаются в посторонней помощи и уходе 78%, а спустя 2 года – 65% [7].
Клинический пример. В клинику обратилась пациентка М-ва 58 лет, в постменопаузе с жалобами, типичными для гипотиреоза. После УЗИ и гормонального исследования функционального состояния ЩЖ был выставлен клинический диагноз: Диффузно-узловой зоб III степени. Гипотиреоз. При комплексном обследовании (ФСГ, ЛГ, ПРЛ, Е2, П, ДЭРА, костный метаболизм, кальций-фосфорный обмен), направленном на выявление климактерических расстройств, установлено: постменопауза, климактерический синдром средней степени тяжести, УГР-II и начальные признаки остеопении в L1-L4. Женщине была назначена терапия, включающая в себя «Остеомед Форте».
При контрольном определении как маркеров костного ремоделирования, так и МПК через год, нами не были установлены костно-метаболические изменения (повышение уровня СТХ, КЩФ и ОК), свидетельствующие о прогрессировании ОП, а имеющие место остеопенические нарушения не только не прогрессировали, но и подвергались регрессии, достигнув значений, характерных для здоровых женщин этого же возраста.
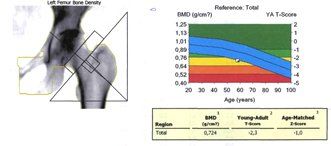
а)
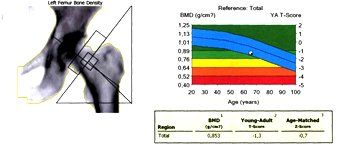
b)
Рисунок 2. Денситометрические показатели МПК – исходно (а) и после терапии препаратом Остеомед Форте (b) в Troch
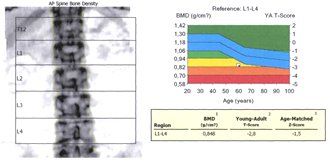
а)
b)
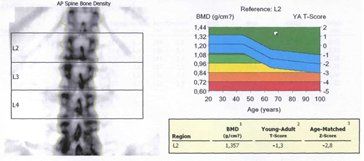
Рисунок 3. Денситометрические показатели МПК – исходно (а) и после терапии препаратом Остеомед Форте (b) в L1-L4
а)
b)
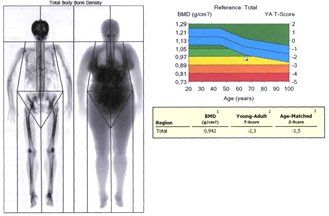
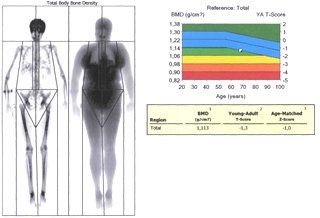
Рисунок 4. Денситометрические показатели МПК – исходно (а) и после терапии препаратом Остеомед Форте (b) в Total body
На фоне терапии обоими препаратами произошла нормализация показателей кальций-фосфорного обмена, в том числе и снижение в крови уровня таких маркеров резорбции кости как Са/кр, Р/кр и ОПР/кр. Прогрессивное возрастание кальцитонина в процессе терапии также является одним из факторов, способствующих снижению интенсивности костных потерь и нормализации костного метаболизма у пациенток с патологий щитовидной железы в постменопаузе (таблица 3).
Таблица 3.
Динамика показателей кальций-фосфорного обмена и некоторых биохимических маркеров костного метаболизма на фоне двух видов терапии (М±m)
| Маркер | Исходный уровень | 1 подгруппа (N=82) | 2 подгруппа (N=83) |
| Са2+ (ммоль/л) | 1,07±0,01 | 1,18±0,05 | 1,31±0,05 |
| Р (ммоль/л) | 0,98±0,02 | 1,17±0,04 | 1,18±0,03 |
| Са/кр (мкм/мкм. кр.) | 0,9±0,06 | 0,63±0,02* | 0,54±0,03* |
| Р/кр (мкм/мкм. кр.) | 2,96±0,13 | 2,94±0,1 | 2,78±0,12 |
| ОПР/кр (мкм/мкм. кр.) | 3,97±0,09 | 1,60±0,07* | 1,71±0,09* |
| ПТГ (pg/ml) | 53,24±2,03 | 48,1±2,05 | 48,6±2,3 |
| КТ (пг/мл) | 3,1±1,02 | 4,7±1,04* | 4,9±1,2* |
Примечание: * – различия с контрольной группой достоверны (р<0,05)
В результате проведенного исследования установлено, что на фоне терапии обоими препаратами произошло снижение уровней маркеров костного ремоделирования (таблица 4). Так, на фоне приема препарата Анжелик (1-ая подгруппа пациенток) СТХ в сыворотке крови составила 0,296±0,03, в моче – 173,2±145, в то время как, на фоне приема Остеомеда Форте (2-ая подгруппа) СТХ в сыворотке крови – 0,335±0,07, а в моче – 195,2±128. Данные говорят о высоком антирезорбтивном эффекте обоих препаратов.
Таблица 4.
Динамика маркеров костного ремоделирования на фоне двух видов терапии (М±m)
| Маркер | Исходно | 12 месяцев | |
| 1 подгруппа (N=82) | 2 подгруппа (N=83) | ||
| СТХ в сыворотке крови (нг/мл) | 0,624±0,06 | 0,296±0,03* | 0,335±0,07* |
| СТХ в моче (мкг/моль. кр.) | 425,5±142,0 | 173,2±145* | 195,2±128* |
| КЩФ (Ед/л) | 38,5±2,5 | 24,2±4,1* | 32,5±1,9* |
| ОК (ng/ml) | 11,42±1,05 | 6,42±0,71* | 9,0±1,05* |
Примечание: * – различия с контрольной группой достоверны (р<0,05)
Резюме
Таким образом, как при патологии тиреоидной системы, так и без нее, терапия препаратами Анжелик и Остеомед Форте оказывает выраженный блокирующий эффект на костную резорбцию у женщин с постменопаузальной остеопенией и ОП.
При этом, что касается маркеров образования кости, а именно КЩФ и ОК, то на фоне терапии Остеомед Форте стимуляция этих показателей была более выраженной (КЩФ – 32,5±1,9; ОК – 9,0±1,05), чем на фоне приема препарата Анжелик (КЩФ – 24,2±4,1; ОК – 6,42±0,71), что, возможно, и обусловило более выраженный протективный эффект (5,5%) Остеомеда Форте на минеральную плотность кортикальной кости. Таким образом, Остеомед Форте может служить препаратом выбора для лечения остеопенических проявлений у больных с ранним поражением не только трабекулярной, но и кортикальной кости.
Немаловажным фактом является и то, что активное биологическое вещество «трутневый расплод» в составе препарата Остеомед Форте благотворно влияет на функцию щитовидной железы, в том числе и при гипотиреозе, что нашло подтверждение и у наших пациенток, которые отмечали улучшение самочувствия, связанного с патологией щитовидной железы на фоне приема данного препарата.
Резюмируя вышеизложенное, можно сделать следующие выводы:
- Остеомед Форте может служить препаратом выбора для лечения остеопенических проявлений у больных с патологией тиреоидной системы в постменопаузе, показывая выраженный положительный эффект на минеральную плотность кости (5,5%). Это коррелирует со снижением резорбционной активности биохимических маркеров костного ремоделирования на 50,2%.
- Позитивными сторонами использования данного препарата у больных в постменопаузе с патологией тиреоидной системы, является то, что, во-первых, Остеомед Форте не оказывает таких серьезных побочных эффектов, присущих МГТ, как венозная тромбоэмболия, рак молочной железы, артериальный тромбоз и др., что делает его приемлемым для длительного применения и, во-вторых, благотворно влияет на функцию щитовидной железы и на климактерические расстройства.
Учитывая, выраженный протективный эффект препарата Остеомед Форте в отношении кортикальных структур скелета (проксимальный отдел бедра – 4,4±0,2%, дистальный отдел предплечья – 4,3±0,1%), Остеомед Форте рекомендован не только с лечебной, но и с профилактической целью у женщин в постменопаузе с компенсированным гипотиреозом, что позволит снизить летальность при переломах шейки бедра у данного контингента пациенток.
Список литературы:
- Подзолкова Н.М., Кузнецова И.В., Никитина Т.И. Менопаузальный остеопороз. Руководство для врачей. М: ГЭОТАР – Медиа 2012, стр 5-10.
- Дедов И.И., Свириденко И.Ю. Стратегия ликвидации йоддефицитных заболеваний в Российской Федерации // Проблемы эндокринологии. – 2001. – Т.47. – №6. – С. 3-12.
- Baran D. Braverman L.E. Thyroid hormone and bone mass // J. Clin Endocrinol. Metab. – 1991. – V.72. – P.1182-1183.
- Тюрин Ю.И., Макарова А.А. Анализ данных на компьютере. М: Мысль 2003; 280с.
- Поляков И.В., Соколова И.С. Практическое пособие по медицинской статистике. Л: Крон-пресс 1995; 148с.
- Duncan W.T., Solomon B. Influence of clinical characteristics and parameters associated with thyroid hormone therapy on the bone mineral density of women treated with thyroid hormone // Thyroid. – 1994. – V.4. – P. 183-190.
- Меньшикова Л.В., Храмцова Н.А., Ершова О.Б. Ближайшие и отдаленные исходы переломов проксимального отдела бедра у лиц пожилого возраста и их медико-социальные последствия (по данным многоцентрового исследования). Остеопороз и остеопатии 2002;1:8–11.












2 комментария